*Я подтверждаю, что являюсь специалистом сферы здравоохранения

Добавлено: 17 Февраля 2025
Одобрение Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) золбетуксимаба в сочетании с химиотерапией в октябре 2024 года изменило ландшафт лечения рака желудка. Однако, исследование REFLECT, проведенное за несколько месяцев до его одобрения, показало пробел в знаниях среди онкологов о клаудине 18.2 (CLDN18.2), мишени, на которую действует препарат.

Добавлено: 03 Февраля 2025
Китайские исследователи провели открытое многоцентровое клиническое исследование II фазы CT041-ST-01 (NCT04581473), в котором оценивается безопасность и эффективность препарата satricabtagene autoleucel (Satri-cel, CT041). Это аутологичный CAR-T-клеточный продукт против Claudin18.2, который назначался пациентам с Claudin18.2-положительным прогрессирующим раком желудка/желудочно-пищеводного перехода после 2-й и более линий терапии.
Добавлено: 27 Января 2025
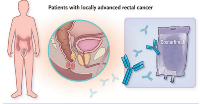
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) присвоило достарлимабу статус прорывной терапии для лечения пациентов с местнораспространенным раком прямой кишки с дефицитом репарации несоответствия (dMMR) и высоким уровнем микросателлитной нестабильности (MSI-H). Обозначение прорывной терапии направлено на ускорение разработки и одобрения препаратов с потенциалом для лечения серьезного заболевания и в тех случаях, когда предварительные клинические данные указывают на существенное улучшение результатов по сравнению с доступной в настоящее время терапией.

Добавлено: 13 Января 2025
При прогрессирующей протоковой аденокарциноме поджелудочной железы (PDAC) химиотерапия 1-й линии является стандартом лечения. В связи с отсутствием прямых сравнений в клинических исследованиях проведен систематический обзор и метаанализ всех вариантов лечения PDAC с точки зрения их эффективности и токсичности.
Добавлено: 23 Декабря 2024
Рекомендации по лечению метастатического колоректального рака (мКРР) не зависят от возрастной группы. Тем не менее, агрессивная многокомпонентная химиотерапия, включающая FOLFOXIRI+бевацизумаб (триплет+бев), обычно назначается пациентам более молодого возраста. Проведено ретроспективное исследование, основанное на реальных данных, в котором оценивалось применение триплета с бевацизумабом у пациентов с мКРР в разных возрастных группах.

Добавлено: 09 Декабря 2024
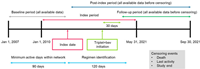
Рак прямой кишки ранней стадии (EORC) характеризуется уникальными клинико-патологическими особенностями, отличающимися от рака прямой кишки на поздней стадии (LORC). Авторы нового исследования радиомики разработали прогностическую модель для точного определения риска рецидива при EORC.

Добавлено: 09 Декабря 2024
Большое количество доказательств, свидетельствующих о связи между большим объемом хирургических операций и лучшими периоперационными результатами, в том числе при сложных онкологических операциях, поддерживает идею централизации такой терапии в специализированных центрах, которые соответствуют пороговым значениям хирургического объема. Тем не менее, большое расстояние до этих центров свидетельствует о потенциальном неравенстве в доступе к качественной онкологической помощи.
Добавлено: 02 Декабря 2024
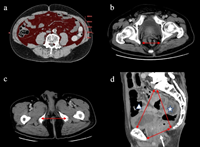
Согласно исследованию, опубликованному 27 сентября в BMC Gastroenterology, висцеральный жир нижней части живота (VFA), пожилой возраст и длительная операция являются независимыми факторами риска развития послеоперационного нейрогенного мочевого пузыря (PONB) после операции по удалению рака прямой кишки (РПК).

Добавлено: 18 Ноября 2024
Неоадъювантное применение ингибиторов контрольных точек иммунного ответа (ИКТ) перед резекцией печени приводит к регрессу опухоли у пациентов с гепатоцеллюлярной карциномой (ГЦК). D'Alessio Antonio с соавт. провели исследование, целью которого было описать характеристики патологических ответов после предоперационной терапии ИКТ при ГЦК и оценить связь между глубиной регрессии опухоли и безрецидивной выживаемостью (БРВ).
Добавлено: 04 Ноября 2024
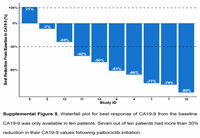
Муцинозные новообразования желудочно-кишечного тракта характеризуются склонностью к метастазированию в брюшину, что приводит к перитонеальному муцинозному карциноматозу (ПМК). Подгруппа этих опухолей, чаще всего возникающих в аппендиксе, содержит мутации в онкогене GNAS. Хотя естественное течение ПМК с мутацией GNAS варьирует, результаты лечения пациентов, как правило, неутешительны. Целью опубликованного в Journal of Clinical Oncology исследования была оценка клинической эффективности монотерапии палбоциклибом, ингибитором циклин-зависимой киназы (CDK) 4/6, у пациентов с мутацией GNAS при ПМЛ.














