*Я подтверждаю, что являюсь специалистом сферы здравоохранения

Добавлено: 13 Февраля 2023
Согласно результатам рандомизированного исследования III фазы ASTRUM-005, добавление серплулимаба к химиотерапии (ХТ) улучшает общую выживаемость у пациентов с ранее нелеченным мелкоклеточным раком легкого(МКРЛ)...

Добавлено: 23 Января 2023
Прецизионная медицина продемонстрировала большой потенциал для улучшения результатов лечения и продления выживаемости пациентов с раком легкого (РЛ). По данным Международной ассоциации по изучению рака легкого, более половины пациентов имеют опухоли, содержащие потенциально активные драйверные мутации. Согласно исследованию Deb D и соавт, опубликованному в Journal of Thoracic Oncology, методы лечения, нацеленные на эти мутации, (ALK, BRAF, EGFR, HER2, RET, KRAS и BRAF и другие), в настоящее время, доминируют в области лечения РЛ. Использование таргетной терапии может значительно продлить выживаемость по сравнению цитотоксической химиотерапией...

Добавлено: 23 Января 2023
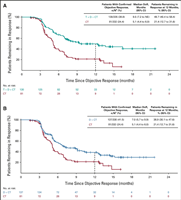
Согласно результатам исследования II фазы, опубликованным на платформе JAMA Oncology, добавление атезолизумаба к бевацизумабу показало многообещающую эффективность среди пациентов с неплоскоклеточным немелкоклеточным раком легкого (НМРЛ) с высокой мутационной нагрузкой...

Добавлено: 23 Января 2023
В декабре 2022г обновлены 2 рекомендации по терапии распространенного немелкоклеточного рака легкого (НМРЛ)...
Добавлено: 19 Декабря 2022
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило применение тремелимумаба в комбинации с дурвалумабом и химиотерапией (ХТ) на основе платины для некоторых пациентов с метастатическим немелкоклеточным раком легкого (НМРЛ)...
Добавлено: 28 Ноября 2022
Согласно результатам японского проспективного исследования, представленного на Всемирном конгрессе по борьбе с раком, более низкий индекс массы тела (ИМТ) может увеличить риск развития рака легких (РЛ). Исследователи пришли к выводу, что отказ от курения и поддержание соответствующей массы тела являются критическими факторами для профилактики РЛ...
Добавлено: 24 Октября 2022
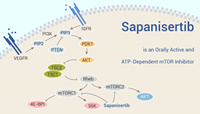
FDA присвоило сапанисертибу статус ускоренного одобрения для лечения взрослых пациентов с неоперабельным или метастатическим плоскоклеточным немелкоклеточным раком легкого (НМРЛ), опухоли которых содержат мутации ядерного фактора эритроид 2 (NRF2), и которые ранее получали терапию ингибиторами иммунных контрольных точек и химиотерапию на основе препаратов платины...
Добавлено: 03 Октября 2022
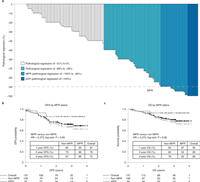
Выживаемость пациентов с резектабельным немелкоклеточным раком легкого (НМРЛ) существенно не улучшилась с момента введения адъювантной химиотерапии (ХТ) в качестве стандартного лечения более 20 лет назад. Ингибиторы иммунных контрольных точек PD- (L) 1 одобрены для лечения прогрессирующего НМРЛ и резецированного НМРЛ II–III стадии, экспрессирующего PD-L1 НМРЛ...

Добавлено: 26 Сентября 2022
Соторасиб, пероральный необратимый ингибитор KRAS G12C, одобрен для лечения пациентов с прогрессирующим НМРЛ с мутацией KRAS G12C...

Добавлено: 29 Августа 2022
Обновлены и опубликованы 11 июля 2022 рекомендации Американской ассоциации клинических онкологов (ASCO) по терапии немелкоклеточного рака легких (НМРЛ) на основе продолжающегося систематического обзора рандомизированных клинических исследований с 2018 по 2021 год...














