*Я подтверждаю, что являюсь специалистом сферы здравоохранения

Добавлено: 09 Января 2023
22 декабря 2022г FDA одобрен мосунетузумаб для лечения взрослых пациентов с рецидивирующей или рефрактерной фолликулярной лимфомой (ФЛ) после двух или более линий системной терапии...

Добавлено: 19 Декабря 2022
Пациенты с агрессивной В-клеточной лимфомой и перегруппировкой MYC имеют плохой прогноз при использовании стандартного режима R-CHOP (ритуксимаб, циклофосфамид, доксорубицин, винкристин, преднизолон). В 5 итальянских центрах 68 пациентов с лимфомой Беркитта (BL; n = 46) или В-клеточной лимфомой высокой степени злокачественности (HGBCL; n = 22) получали кратковременную дозоинтенсивную терапию CARMEN. 46 (68%) пациентов были ВИЧ-инфицированы. Режим CARMEN включал 36-дневную индукцию с последовательным однократным еженедельным введением циклофосфамида, винкристина, ритуксимаба, метотрексата, этопозида и доксорубицина плюс интратекальную химиотерапию с последующей консолидацией на основе высокодозного цитарабина. Пациенты, которые не достигли полной ремиссии (ПР) после индукции, получали ВЕАМ (кармустин, этопозид, цитарабин, мелфалан) и аутологичную трансплантацию стволовых клеток (ауто-ТГСК). 61 (90%) пациент завершил индукцию, а 59 (87%) завершили консолидацию. 17 больных получили ауто-ТГСК. Гематологическая токсичность 4 степени была распространенной, но не приводила к прекращению лечения; негематологическая токсичность 4 степени была зарегистрирована у 11 (16%) пациентов, а инфекции 4 степени - у 6 (9%)...
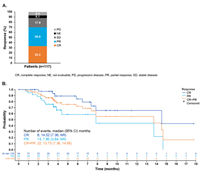
Добавлено: 05 Декабря 2022
Исследование II фазы демонстрирует высокую частоту объективных ответов при использовании камиданлумаба тесирина у пациентов с рецидивирующей или рефрактерной классической лимфомой Ходжкина (Р/Р ЛХ), получавших интенсивное предшествующее лечение...
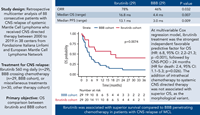
Добавлено: 14 Ноября 2022
Рецидив мантийноклеточной лимфомы (МКЛ) с поражением центральной нервной системы (ЦНС) - редкое явление с крайне неблагоприятным прогнозом, при котором не существует стандартных подходов. Поскольку ковалентный ингибитор тирозинкиназы Брутона (BTK) ибрутиниб эффективен при рецидивирующей / рефрактерной МКЛ и проникает через гематоэнцефалический барьер (ГЭБ), Итальянским фондом Linfomi и Европейской сетью по борьбе с МКЛ было инициировано многоцентровое ретроспективное международное исследование по сравнению результатов лечения таких пациентов ибрутинибом или химиоиммунотерапией...
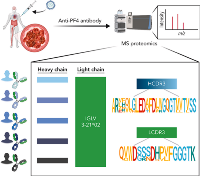
Добавлено: 31 Октября 2022
Синдром вакциноиндуцированной иммунной тромботической тромбоцитопении (VITT) является редким тромбоэмболическим осложнением вакцин аденовирусной направленности ChAdOx1 nCoV-19 (AstraZeneca) и Ad26.COV2.S (Janssen/ Johnson & Johnson)...

Добавлено: 31 Октября 2022
На платформе Blood в октябре 2022г опубликованы результаты рандомизированного плацебо-контролируемого исследования 3 фазы QUAZAR AML-001 (NCT01757535). Пациенты с острым миелоидным лейкозом (ОМЛ), не кандидаты на трансплантацию, в первой ремиссии после интенсивной химиотерапии были рандомизированы 1: 1 для перорального прием азацитидина (Oral-AZA) 300 мг или плацебо в течение 14 дней в течение 28-дневного цикла...
Добавлено: 17 Октября 2022
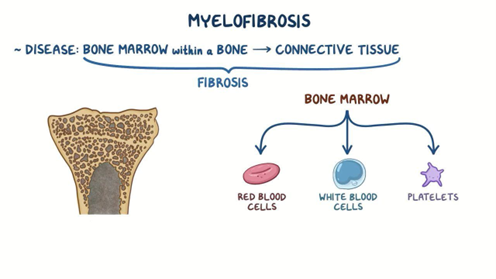
29 сентября 2022 года, биотехнологическая компания, специализирующаяся на разработке новых методов лечения фиброза и рака, объявила о положительных результатах промежуточной оценки продолжающегося исследования фазы 2a лечения миелофиброза GB2064 (MYLOX-1, NCT04679870)...
Добавлено: 10 Октября 2022
За последние несколько лет произошла принципиальная смена парадигмы первой линии терапии хронического лимфоцитарного лейкоза (ХЛЛ). 5-летняя общая выживаемость пациентов с ХЛЛ ежегодно увеличивается, при этом текущие показатели составляют 86,9%. На платформе JCO Oncol Pract опубликован обзор ведущих специалистов в области ХЛЛ - Brem EA, O'Brien S...

Добавлено: 19 Сентября 2022
Результаты продолжающегося исследования I фазы показали, что почти 60% пациентов с активно предлеченной множественной миеломой (ММ) ответили на исследуемое биспецифическое антитело...

Добавлено: 19 Сентября 2022
Периферические Т-клеточные лимфомы представляют гетерогенную группу лимфопролиферативных заболеваний, на долю которых приходится около 10% вновь диагностированных лимфом во всем мире. У взрослых пациентов в настоящее время диагностируется >20 различных подтипов, при этом наиболее распространенными считаются анапластическая крупноклеточная лимфома (ALCL), ангиоиммунобластная Т-клеточная лимфома (AITL) и периферическая Т-клеточная, не уточненная (PTCL NOS). Прогноз пациентов, как правило, неблагоприятный, с медианой 5-летней общей выживаемости (ОВ) от 28% до 32%. Некоторые подтипы PTCL имеют еще более худший прогноз, исключением является ALK + ALCL, с медианой 5-летней ОВ от 70% до 86%...














