*Я подтверждаю, что являюсь специалистом сферы здравоохранения
Добавлено: 24 Января 2022
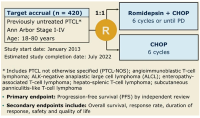
Прогноз при периферической Т-клеточной лимфоме (ПТКЛ) оставляет желать лучшего. В течение последнего десятилетия не удалось улучшить результаты СНОР в первой линии терапии, за исключением новой опции - брентуксимаба ведотина для CD30+ ПТКЛ...
Добавлено: 17 Января 2022
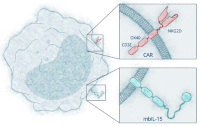
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) присвоило препарату NK101 для лечения острого миелоидного лейкоза (ОМЛ) статус орфанного...
Добавлено: 17 Января 2022
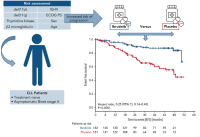
13 января на платформе Blood опубликованы результаты двойного слепого плацебо контролируемого исследования III фазы CLL12, в котором бессимптомные, ранее нелеченные пациенты с хроническим лимфолейкозом (ХЛЛ) получали либо ибрутиниб, либо плацебо...

Добавлено: 10 Января 2022
1) Исследование III фазы POLARIX.
2) Исследование III фазы ZUMA-7.
3) Исследование III фазы TRANSFORM.
4) Исследование III фазы BELINDA.

Добавлено: 10 Января 2022
1) Исследование I/II фазы – мосунетузумаб у предлеченных пациентов с фолликулярной лимфомой.
2) Исследование II фазы по CAR Т-терапии при рецидивах ФЛ ELARA.
3) Исследование II фазы CITADEL-203.
Добавлено: 27 Декабря 2021
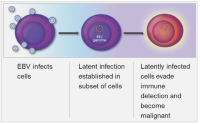
29 ноября 2021 года в Сан-Диего объявлено о том, что FDA предоставило статус орфанного комбинированной этиотропной пероральной терапии нанатиностатом и валганцикловиром для лечения Эпштейн-Барр вирус позитивной диффузной В-крупноклеточной лимфомы, неспецифицированной (ЭБВ ДВКЛ, NOS)...

Добавлено: 27 Декабря 2021
30 ноября 2021 года Управление по контролю за продуктами и лекарствами одобрило режим даратумумаб и карфилзомиб плюс дексаметазон для взрослых пациентов с рецидивирующей или рефрактерной множественной миеломой, которые ранее получали от 1 до 3 линий терапии...

Добавлено: 27 Декабря 2021
На платформе The Lancet в декабре 2021г опубликованы результаты нерандомизированного исследования II фазы, проведенного в двух академических медицинских центрах США. Авторы предположили, что сочетание занубрутиниба с обинутузумабом и венетоклаксом (BOVen) в качестве инициальной терапии хронического лимфоцитарного лейкоза (ХЛЛ) и лимфомы из малых лимфоцитов может привести к высоким показателям неопределяемой минимальной остаточной болезни (MRD)...
Добавлено: 20 Декабря 2021
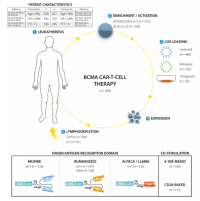
Доктор Richard S. на симпозиуме по химиотерапии «Chemotherapy Foundation Symposium: Innovative Cancer Therapy for Tomorrow» 3–5 ноября 2021г представила пленарный доклад по новым возможностям терапии множественной миеломы (ММ)...

Добавлено: 20 Декабря 2021
В журнале Blood опубликованы результаты рандомизированного исследования III фазы, которые продемонстрировали, что коррекция режима леналидомид плюс дексаметазон (RD), которая включала прекращение приема дексаметазона через 9 месяцев (RD-R), оказался безопасным и привел к тем же результатам, что и непрерывный прием леналидомида и дексаметазона (RD) у пожилых пациентов с множественной миеломой (ММ)...














