*Я подтверждаю, что являюсь специалистом сферы здравоохранения
Добавлено: 25 Марта 2019
21 марта 2019 года Управление по санитарному надору за пищевыми продуктами и медикаментами (Food and Drug Administration, FDA) объявило о приостановке проведения исследования III фазы BELLINI, посвященного изучению эффективности венетоклакса в первой линии терапии множественной миеломы. Венетоклакс (Венклекста, AbbVie) – селективный ингибитор белка BCL-2 (B-cell lymphoma-2 protein), предназначенный для перорального приема. Указанный белок играет важную роль в патогенезе хронического лимфолейкоза и других опухолей кроветворной системы, включая множественную миелому.
Добавлено: 22 Марта 2019
Ибрутиниб (Имбрувика, Janssen/AbbVie) – пероральный ингибитор тирозинкиназы Брутона (ТКБ). ТКБ играет важную роль в путях метаболизма, связанных с сигнальной активностью антигенных рецепторов В-клеток (BCR), а также ряда цитокиновых рецепторов. Сигнальный путь BCR участвует в процессах выживания и миграции В-лимфоцитов в организме человека, а также в патогенезе ряда злокачественных новообразований. 20 марта 2019 года в журнале Journal of Clinical Oncology были опубликованы результаты двойного слепого рандомизированного исследования III фазы, посвященного изучению эффективности добавления ибрутиниба к стандартной терапии первой линии по схеме R-CHOP в лечении пациентов с диффузной В-крупноклеточной лимфомой (ДВКЛ).
Добавлено: 11 Марта 2019
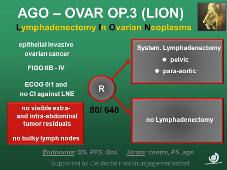
У большинства пациенток рак яичников (РЯ) выявляется на поздних стадиях. Их выживаемость напрямую зависит от качества хирургического лечения – те пациентки, у которых были достигнута полная циторедукция (отсутствие макроскопической остаточной опухоли) имеют наиболее благоприятный прогноз. Именно полная циторедукция декларируется в качестве цели хирургического лечения РЯ. В то же время, роль выполнения забрюшинной лимфодиссекции при этом заболевании в течение долго времени оставалась спорной.
Добавлено: 07 Марта 2019
Авелумаб (Бавенсио, Pfizer) – моноклональное антитело к лиганду сигнального пути программируемой клеточной гибели (Programmed cell Death Pathway Ligand, PD-L1), экспрессия которого обнаруживается на поверхности опухолевых клеток и инфильтрирующих иммунных клеток. Акситиниб (Инлита, Pfizer) – селективный ингибитор рецепторов сигнального пути фактора роста эндотелия (VEGFR), препарат также подавляет активность c-KIT и PGFR [1].
Добавлено: 06 Марта 2019
Иммунотерапия - это настоящая революция в лечении онкологических заболеваний. PD-1 ингибиторы уже активно используются как в мировой, так и в российской практике и являются стандартом в лечении целого ряда онкологических заболеваний....

Добавлено: 25 Февраля 2019
Антрациклин-содержащие режимы химиотерапии (AC/FAC, EC/FEC) являются текущим стандартом адъювантной терапии рака молочной железы (РМЖ). Они характеризуются высокой эффективностью, но их применение сопряжено с повышением риска развития долговременных нежелательных явлений, в первую очередь – сердечной недостаточности, связанной с кардиотоксичностью антрациклинов.
Добавлено: 22 Февраля 2019
Стандарт адъювантной терапии пациенток с ранними стадиями гормонозависимого (ГР+) рака молочной железы (РМЖ) в постменопаузе – применение ингибиторов ароматазы. Они позволяют значительно снизить вероятность рецидива, но увеличивают риск остеопороза и связанных с ним патологических переломов. Результаты ранее проведенного исследования ABCSG-18 показали, что применение деносумаба в сочетании с ингибиторами ароматазы значительно уменьшает риск патологических переломов.

Добавлено: 22 Февраля 2019
В последние десятилетия спектр возможностей терапии лимфопролиферативных заболеваний стал невероятно широким. Он включает в себя цитостатическую терапию, лучевую терапию, таргетную терапию, аутологичную и аллогенную трансплантацию гемопоэтических стволовых клеток (ТГСК) и иммунотерапию. Это делает принятие решения об оптимальной стратегии лечения онкогематологических пациентов сложной комплексной задачей для междисциплинарной команды специалистов – онкогематологов, патоморфологов, лучевых терапевтов, нередко – экспертов смежных специальностей (кардиологов, инфекционистов и других). Правильное решение этой задачи как правило может позволить значительно продлить жизнь пациенту. Это делает очень важным обмен опытом между экспертами федеральных центров и специалистов региональных клиник для более эффективного внедрения новых возможностей диагностики и лечения на практике.
Добавлено: 21 Февраля 2019
Тамоксифен – один из наиболее часто применяемых препаратов для лечения гормонозависимого (ГР+) рака молочной железы (РМЖ). Этот препарат является пролекарством и требует активации в печени, которая осуществляется при участии изофермента CYP2D6; его активный метаболит – эндоксифен (Рисунок 1). Предполагается, что концентрация эндоксифена может быть предиктором эффективности терапии тамоксифеном.
Добавлено: 13 Февраля 2019
Акситиниб (Инлита, Pfizer) – селективный ингибитор рецепторов сигнального пути фактора роста эндотелия (VEGFR), препарат также подавляет активность c-KIT и PGFR. Пембролизумаб (Китруда, Merck) – моноклональное антитело к рецептору сигнального пути программируемой клеточной гибели (Programmed cell Death Pathway Ligand, PD-1), экспрессия которого обнаруживается на поверхности опухолевых клеток и инфильтрирующих иммунных клеток. Опухолевые клетки способны использовать этот сигнальный путь для ухода от надзора иммунной системы организма. Результаты ранее проведенных исследований продемонстрировали наличие синергизма между акситинибом и препаратами, воздействующими на сигнальный путь PD-L1/PD-L1 [1].
- Предыдущая
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 29
- 30
- 31
- 32
- 33
- 34
- 35
- 36
- 37
- 38
- 39
- 40
- 41
- 42
- 43
- 44
- 45
- 46
- 47
- 48
- 49
- 50
- 51
- 52
- 53
- 54
- 55
- 56
- 57
- 58
- 59
- 60
- 61
- 62
- 63
- 64
- 65
- 66
- 67
- 68
- 69
- 70
- 71
- 72
- 73
- 74
- 75
- 76
- 77
- 78
- 79
- 80
- 81
- 82
- 83
- 84
- 85
- 86
- 87
- 88
- 89
- 90
- 91
- 92
- 93
- 94
- 95
- 96
- 97
- 98
- 99
- 100
- 101
- 102
- 103
- 104
- 105
- 106
- 107
- 108
- 109
- 110
- 111
- 112
- 113
- 114
- 115
- 116
- 117
- 118
- 119
- 120
- 121
- 122
- 123
- 124
- 125
- 126
- 127
- 128
- 129
- 130
- 131
- 132
- 133
- 134
- 135
- 136
- 137
- 138
- 139
- 140
- 141
- 142
- 143
- 144
- 145
- 146
- 147
- 148
- 149
- 150
- 151
- 152
- 153
- 154
- 155
- 156
- 157
- 158
- 159
- 160
- 161
- 162
- 163
- 164
- 165
- 166
- 167
- 168
- 169
- 170
- 171
- 172
- 173
- 174
- 175
- 176
- 177
- 178
- 179
- 180
- 181
- 182
- 183
- 184
- 185
- 186
- 187
- 188
- 189
- 190
- Следующая














