*Я подтверждаю, что являюсь специалистом сферы здравоохранения
Добавлено: 08 Сентября 2025
Результаты китайского одноцентрового исследования II фазы (SPRING-01), опубликованные на платформе The Lancet Oncology, показали, что добавление ингибитора PD-1 синтилимаба к химиотерапии (ХТ) после короткого курса лучевой терапии в рамках неоадъювантного лечения значительно увеличивает частоту полного патоморфологического ответа у пациентов с местнораспространённым раком прямой кишки (РКП).
Добавлено: 08 Сентября 2025
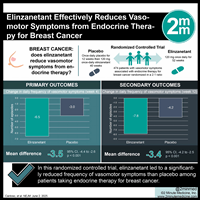
У женщин, получающих эндокринную терапию при гормонозависимом (HR+) раке молочной железы (РМЖ), часто наблюдаются вазомоторные симптомы. Опубликованы результаты исследования III фазы с участием женщин в возрасте от 18 до 70 лет с вазомоторными симптомами средней и высокой степени тяжести, связанными с эндокринной терапией HR+РМЖ. Женщины были рандомизированы в соотношении 2:1 в группы, получавшие элинзанетант в дозе 120 мг один раз в день в течение 52 недель или плацебо один раз в день в течение 12 недель, после чего элинзанетант в дозе 120 мг один раз в день в течение 40 недель. Основными конечными точками были изменения суточной частоты вазомоторных симптомов средней и высокой степени тяжести по сравнению с исходным уровнем на 4-й и 12-й неделях.

Добавлено: 01 Сентября 2025
На платформе The Lancet опубликованы результаты исследования III фазы KRYSTAL-12, которые продемонстрировали преимущество адаграсиба по сравнению с доцетакселом в отношении ВБП у пациентов с ранее леченным местнораспространенным или метастатическим немелкоклеточным раком легкого (НМРЛ) с мутацией в KRAS G12C.

Добавлено: 01 Сентября 2025
Во франко-бельгийском исследовании III фазы (ASTER 70s), результаты которого были опубликованы на платформе The Lancet, изучали влияние адъювантной химиотерапии (аХТ) на выживаемость женщин в возрасте ≥ 70 лет с рецептор-положительным, HER2-отрицательным раком молочной железы (РМЖ) с высоким генетическим риском по шкале GGI.

Добавлено: 01 Сентября 2025
Одобренные ингибиторы контрольных точек (ИКТ) ниволумаб и пембролизумаб демонстрируют высокие показатели ответа при рецидивирующей/рефрактерной лимфоме Ходжкина (ЛХ), но не приводят к полному излечению, в то время как аллогенная трансплантация стволовых гемопоэтических клеток (аллоТГСК) позволяет излечить >50% пациентов. Чтобы оценить влияние предварительной терапии ИКТ, Perales с соавт. проанализировали данные 2186 взрослых пациентов с рецидивом ЛХ, которым провели аллоТГСК, и обнаружили, что, несмотря на большую частоту острой реакции трансплантат против хозяина (РТПХ), чем у тех, кто не получал терапию ИКТ, ВБП была выше у пациентов с предшествующим ИКТ. Авторы также оценили использование посттрансплантационного циклофосфамида для профилактики РТПХ.
Добавлено: 01 Сентября 2025
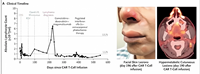
На платформе The New England Journal of Medicine описан случай успешного таргетного лечения периферической Т-клеточной лимфомы, развившейся после CAR-Т-клеточной терапии множественной миеломы (ММ).

Добавлено: 01 Сентября 2025
Согласно результатам исследования A. Claudel с соавт., только сочетание уровня циркулирующей опухолевой ДНК (цДНК) и метаболического ответа после 1-йI линии терапии по данным ПЭТ позволяет выявить пациентов с высоким риском раннего рецидива (POD24) при фолликулярной лимфоме (ФЛ).

Добавлено: 01 Сентября 2025
Опубликованы результаты рандомизированного исследования III фазы, в рамках которого пациенты с локально распространенной плоскоклеточной карциномой кожи высокого риска, после хирургической резекции и послеоперационной лучевой терапии, были рандомизированы в соотношении 1:1 для получения адъювантной терапии цемиплимабом (350 мг) или плацебо, вводимых внутривенно каждые 3 недели в течение 12 недель, с последующим увеличением дозы до 700 мг, вводимых каждые 6 недель в течение 36 недель (всего ≤48 недель). Первичной конечной точкой стала ВБП заболевания. Вторичными конечными точками стали отсутствие локорегионарных рецидивов, отдалённых метастазов и безопасность.

Добавлено: 28 Августа 2025
Профессиональный путь Евгения Александровича был неразрывно связан с Онкологическим центром им. Н. Н. Блохина, которому он посвятил без малого 50 лет жизни. Пройдя путь от врача-онколога до руководителя ведущего профильного отдела, он внес неоценимый вклад в развитие отечественной онкогематологии своими фундаментальными научными исследованиями и многолетней клинической практикой.

Добавлено: 25 Августа 2025
На платформе The Journal of the National Cancer Institute опубликованы результаты анализа Норвежского онкологического регистра, включившего данные о 13 811 женщинах, у которых в период с 2008 по 2020 гг был диагностирован рак молочной железы (РМЖ) на ранней стадии. Этим женщинам были назначены противорвотные препараты и химиотерапия. За всеми пациентками велось наблюдение на предмет метастазирования и смерти до конца 2021 года.
- Предыдущая
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 29
- 30
- 31
- 32
- 33
- 34
- 35
- 36
- 37
- 38
- 39
- 40
- 41
- 42
- 43
- 44
- 45
- 46
- 47
- 48
- 49
- 50
- 51
- 52
- 53
- 54
- 55
- 56
- 57
- 58
- 59
- 60
- 61
- 62
- 63
- 64
- 65
- 66
- 67
- 68
- 69
- 70
- 71
- 72
- 73
- 74
- 75
- 76
- 77
- 78
- 79
- 80
- 81
- 82
- 83
- 84
- 85
- 86
- 87
- 88
- 89
- 90
- 91
- 92
- 93
- 94
- 95
- 96
- 97
- 98
- 99
- 100
- 101
- 102
- 103
- 104
- 105
- 106
- 107
- 108
- 109
- 110
- 111
- 112
- 113
- 114
- 115
- 116
- 117
- 118
- 119
- 120
- 121
- 122
- 123
- 124
- 125
- 126
- 127
- 128
- 129
- 130
- 131
- 132
- 133
- 134
- 135
- 136
- 137
- 138
- 139
- 140
- 141
- 142
- 143
- 144
- 145
- 146
- 147
- 148
- 149
- 150
- 151
- 152
- 153
- 154
- 155
- 156
- 157
- 158
- 159
- 160
- 161
- 162
- 163
- 164
- 165
- 166
- 167
- 168
- 169
- 170
- 171
- 172
- 173
- 174
- 175
- 176
- 177
- 178
- 179
- 180
- 181
- 182
- 183
- 184
- 185
- 186
- 187
- 188
- 189
- 190
- 191
- 192
- 193
- 194
- 195
- 196
- 197
- 198
- 199
- 200
- 201
- 202
- 203
- 204
- 205
- 206
- 207
- 208
- 209
- 210
- 211
- 212
- Следующая














