*Я подтверждаю, что являюсь специалистом сферы здравоохранения
Добавлено: 21 Апреля 2025
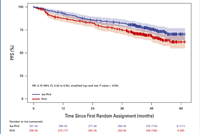
При ранних анализах исследования GMMG-HD7 было показано, что добавление изатуксимаба (Isa) к стандартному лечению леналидомид-бортезомиб-дексаметазон (RVd) у пациентов, подлежащих трансплантации, с впервые диагностированной множественной миеломой приводит к значительному увеличению показателей МОБ-негативности после индукционной терапии. К настоящему времени опубликованы обновленные результаты части 1 исследования.
Добавлено: 21 Апреля 2025
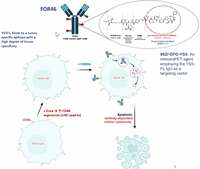
FOR46, полностью человеческое антитело, конъюгированное с монометилауристатином Е, нацелено на опухолевый эпитоп CD46, который сверхэкспрессируется при метастатическом кастрационно-резистентном раке предстательной железы (мКРРПЖ). FOR46 демонстрирует высокую доклиническую активность на энзалутамид-резистентных моделях КРРПЖ.
Добавлено: 21 Апреля 2025
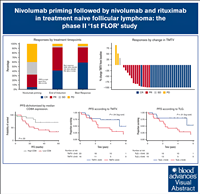
В последнее время появляется все больше доказательств в поддержку иммунного прайминга с использованием PD-1 ингибиторов перед таргетной терапией. В многоцентровом исследовании II фазы FLOR приняли участие 39 пациентов с ранее не леченной прогрессирующей фолликулярной лимфомой (ФЛ). Лечение включало четыре цикла ниволумаба (240 мг), затем четыре 2-недельных цикла ниволумаб + ритуксимаб 375 мг/м2 (индукция), затем 1 год ежемесячного ниволумаба (480 мг) + 2 года поддерживающей терапии ритуксимабом раз в 2 месяца. Участники с полной ремиссией (ПР) после прайминга ниволумабом продолжили монотерапию ниволумабом.

Добавлено: 17 Апреля 2025
Научно-исследовательские проекты в онкологии и гематологии открывают новые возможности в терапии пациентов. В данных областях медицины за период с февраля 2025 по март 2025 гг. на территории РФ были инициированы следующие клинические исследования:

Добавлено: 14 Апреля 2025
Опубликованы данные ретроспективного наблюдательного когортного исследования, проведенного с января 2011 года по октябрь 2022 года, которое включало пациентов, получавших ингибиторы контрольных точек (ИКТ) и госпитализированных с иммуноопосредованными нежелательными явлениями (ИОНЯ). Конечными точками исследования стали: (1) частота госпитализаций с ИОНЯ через 0-6 мес. (ранние), через 6-12 мес. (промежуточные) и более чем через 12 мес. (поздние) после начала терапии ИКТ и (2) оценка факторов, связанных с риском развития ИОНЯ с поздним началом.
Добавлено: 14 Апреля 2025
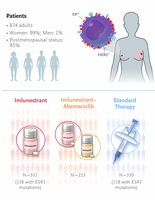
Имлунестрант — это проникающий через гематоэнцефалический барьер пероральный селективный ингибитор рецепторов эстрогенов (ER) нового поколения, который обеспечивает постоянное ингибирование ER даже при опухолях с мутациями в гене, кодирующем ERα (ESR1).
Добавлено: 14 Апреля 2025
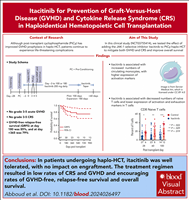
Гаплоидентичная трансплантация гемопоэтических стволовых клеток (haplo-HCT) с посттрансплантационным циклофосфамидом используется все чаще, но такие осложнения, как реакция «трансплантат против хозяина» (РТПХ) и «синдром высвобождения цитокинов» (CRS), остаются серьезными проблемами. Abboud c соавт. сообщают об эффективности добавлении ингибитора JAK1 итацитиниба в стандартный режим профилактики РТПХ после haplo-HCT у 42 пациентов.

Добавлено: 14 Апреля 2025
В 2005 году в исследовании Европейской педиатрической группы по изучению саркомы мягких тканей (EpSSG) оценивалась поддерживающая химиотерапия при рабдомиосаркоме высокого риска. Пациенты были рандомизированы в группы либо для прекращения лечения (стандартная группа), либо для получения шести 28-дневных циклов винорелбина (25 мг/м2) один раз в сутки в 1, 8 и 15 дни, плюс 1 раз в сутки низкие дозы циклофосфамида (25 мг/м2) (экспериментальная группа).
Добавлено: 14 Апреля 2025
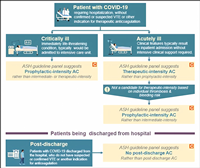
Пациенты с активной инфекцией COVID-19 имеют повышенный риск венозной тромбоэмболии (ВТЭ). Опубликованы научно обоснованные рекомендации Американского общества гематологов (ASH), которые предназначены для принятия решений о применении антикоагулянтов для тромбопрофилактики у пациентов с критическим течением COVID-19; пациентов с острым течением COVID-19; и тех, кто выписывается из стационара без подозреваемой или подтвержденной ВТЭ.
Добавлено: 14 Апреля 2025
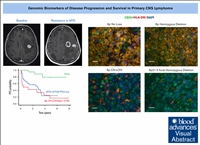
Генетические подтипы первичной лимфомы центральной нервной системы (ПЛЦНС) и их связь с разноплановым ответом на химиоиммунотерапию не установлены. Существует особая потребность в биомаркерах, которые идентифицируют пациентов с впервые диагностированной ПЛЦНС с высоким риском раннего прогрессирования и смерти. Huimin Geng с соавт. применили таргетное секвенирование нового поколения для выявления рецидивирующих однонуклеотидных вариантов, изменений числа копий и аномалий зиготности в диагностических образцах у 78 пациентов с ПЛЦНС, получавших стандартный режим на основе метотрексата, для выявления прогностически значимых молекулярных подгрупп.
- Предыдущая
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 29
- 30
- 31
- 32
- 33
- 34
- 35
- 36
- 37
- 38
- 39
- 40
- 41
- 42
- 43
- 44
- 45
- 46
- 47
- 48
- 49
- 50
- 51
- 52
- 53
- 54
- 55
- 56
- 57
- 58
- 59
- 60
- 61
- 62
- 63
- 64
- 65
- 66
- 67
- 68
- 69
- 70
- 71
- 72
- 73
- 74
- 75
- 76
- 77
- 78
- 79
- 80
- 81
- 82
- 83
- 84
- 85
- 86
- 87
- 88
- 89
- 90
- 91
- 92
- 93
- 94
- 95
- 96
- 97
- 98
- 99
- 100
- 101
- 102
- 103
- 104
- 105
- 106
- 107
- 108
- 109
- 110
- 111
- 112
- 113
- 114
- 115
- 116
- 117
- 118
- 119
- 120
- 121
- 122
- 123
- 124
- 125
- 126
- 127
- 128
- 129
- 130
- 131
- 132
- 133
- 134
- 135
- 136
- 137
- 138
- 139
- 140
- 141
- 142
- 143
- 144
- 145
- 146
- 147
- 148
- 149
- 150
- 151
- 152
- 153
- 154
- 155
- 156
- 157
- 158
- 159
- 160
- 161
- 162
- 163
- 164
- 165
- 166
- 167
- 168
- 169
- 170
- 171
- 172
- 173
- 174
- 175
- 176
- 177
- 178
- 179
- 180
- 181
- 182
- 183
- 184
- 185
- 186
- 187
- 188
- 189
- 190
- 191
- 192
- 193
- 194
- 195
- 196
- 197
- 198
- 199
- 200
- 201
- 202
- 203
- 204
- 205
- 206
- 207
- 208
- 209
- 210
- 211
- 212
- Следующая














