*Я подтверждаю, что являюсь специалистом сферы здравоохранения

Добавлено: 18 Апреля 2017
Онкология и гематология – одни из самых бурно развивающихся областей медицинских знаний. В течение марта 2017 года на территории Российской Федерации (РФ) были начаты следующие клинические исследования в данных областях медицины:
Добавлено: 11 Апреля 2017
В феврале 2017 года Американское Общество Клинической Онкологии (American Society of Clinical Oncology) опубликовало ежегодный отчет, в котором отражены все основные достижения в области онкологии в 2016 году. Для его составления ASCO отобрало результаты исследований, опубликованные в период с октября 2015 по октябрь 2016 г., которые оказали или могут оказать значимое влияние на выживаемость и качество жизни пациентов [1].

Добавлено: 07 Апреля 2017
Применение атезолизумаба (Тесентрик, Roche) позволяет добиться длительной ремиссии заболевания у части пациенток с рецидивами тройного негативного рака молочной железы (ТН РМЖ), свидетельствуют результаты исследования I фазы, представленного в ходе ежегодной конференции Американской Организации по Изучению Рака (American Association for Cancer Research, AACR). Мероприятие прошло в апреле 2017 года в Вашингтоне (DC) [1].

Добавлено: 04 Апреля 2017
27 марта 2017 года Управление по санитарному надзору за безопасностью и качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) одобрило применение препарата нирапариб (Зеюла, Tesaro) для лечения пациенток с рецидивирующим раком яичников (РЯ). Одобренное показание – поддерживающая терапия пациенток с платино-чувствительными рецидивами РЯ, маточной трубы или первичного рака брюшины у которых был отмечен полный или частичный ответ на фоне платино-содержащей химиотерапии [1].
Добавлено: 31 Марта 2017
Идея о возможности использования собственной иммунной системы организма для борьбы со злокачественными опухолями впервые возникла более 100 лет назад, когда было продемонстрировано, что иммунный ответ на возбудителей инфекционных заболеваний может приводить к противоопухолевому эффекту. Попытки разработать эффективные иммунотерапевтические противоопухолевые препараты предпринимались в течение многих лет, однако, большинство методик оказывались неэффективными в реальной клинической практике и в ряде случаев сопровождались тяжелыми побочными эффектами.

Добавлено: 28 Марта 2017
14 марта 2017 года на конференции Американского Общества Онкогинекологов (Society of Gynecologic Oncology, SGO) были представлены результаты рандомизированного плацебо-контролируемого исследования III фазы SOLO-2, в рамках которого изучалась эффективность применения PARP-ингибитора олапариба (Линпарза, AstraZeneca) в качестве поддерживающей терапии пациенток с платино-чувствительными рецидивами BRCA-ассоциированного рака яичников (РЯ).
Добавлено: 21 Марта 2017
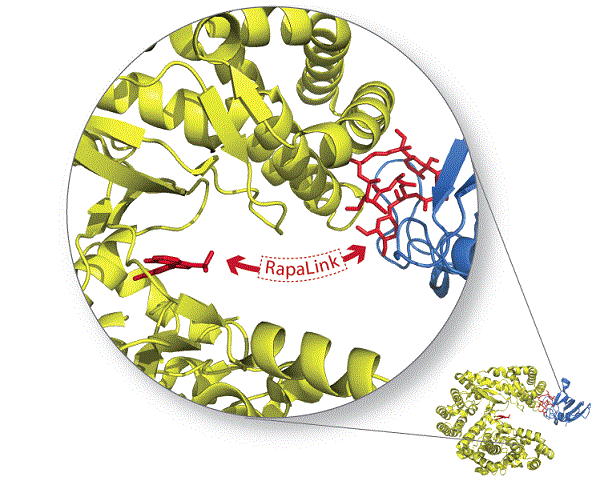
Сигнальный путь PI3K/AKT/mTOR играет важную роль в патогенезе различных злокачественных новообразований, включая рак молочной железы (РМЖ) и почечно-клеточный рак. В настоящее время ингибитор mTOR эверолимус (Афинитор, Novartis) применяется для лечения обоих этих заболеваний. Комбинация эверолимуса и эксеместана (Аромазин, AstraZeneca) продемонстрировала свою эффективность в лечении метастатического гормонозависимого (ГР+) РМЖ и была одобрена для применения у пациенток с прогрессированием заболевания на фоне терапии нестероидными ингибиторами ароматазы летрозолом или анастрозолом.

Добавлено: 20 Марта 2017
13 марта 2017 года Управление по санитарному надзору за безопасностью и качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) одобрило применение рибоциклиба (Кискали, Novartis). Одобренное показание – применение в комбинации с летрозолом в первой линии терапии рака молочной железы (РМЖ) у пациенток с гормонозависимым (ГР+), HER2-негативным подтипом заболевания [1].
Добавлено: 17 Марта 2017
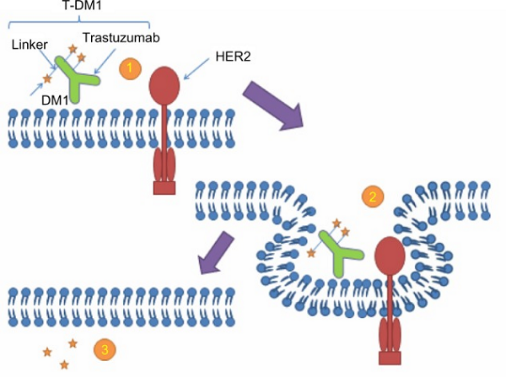
У 15-20% пациенток с операбельными стадиями рака молочной железы (РМЖ) обнаруживается гиперэкспрессия белка HER2-neu (далее HER2), которая ассоциирована с повышением агрессивности течения опухолевого процесса. Стандарт современного лечения данного заболевания – проведение химиотерапии в сочетании с назначением моноклонального антитела к HER2 трастузумаба. Терапию трастузумабом рекомендуется проводить в течение 1 года.

Добавлено: 14 Марта 2017
Онкология и гематология – одни из самых бурно развивающихся областей медицинских знаний. В течение февраля 2017 года на территории Российской Федерации (РФ) были начаты следующие клинические исследования в данных областях медицины:
- Предыдущая
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- 11
- 12
- 13
- 14
- 15
- 16
- 17
- 18
- 19
- 20
- 21
- 22
- 23
- 24
- 25
- 26
- 27
- 28
- 29
- 30
- 31
- 32
- 33
- 34
- 35
- 36
- 37
- 38
- 39
- 40
- 41
- 42
- 43
- 44
- 45
- 46
- 47
- 48
- 49
- 50
- 51
- 52
- 53
- 54
- 55
- 56
- 57
- 58
- 59
- 60
- 61
- 62
- 63
- 64
- 65
- 66
- 67
- 68
- 69
- 70
- 71
- 72
- 73
- 74
- 75
- 76
- 77
- 78
- 79
- 80
- 81
- 82
- 83
- 84
- 85
- 86
- 87
- 88
- 89
- 90
- 91
- 92
- 93
- 94
- 95
- 96
- 97
- 98
- 99
- 100
- 101
- 102
- 103
- 104
- 105
- 106
- 107
- 108
- 109
- 110
- 111
- 112
- 113
- 114
- 115
- 116
- 117
- 118
- 119
- 120
- 121
- 122
- 123
- 124
- 125
- 126
- 127
- 128
- 129
- 130
- 131
- 132
- 133
- 134
- 135
- 136
- 137
- 138
- 139
- 140
- 141
- 142
- 143
- 144
- 145
- 146
- 147
- 148
- 149
- 150
- 151
- 152
- 153
- 154
- 155
- 156
- 157
- 158
- 159
- 160
- 161
- 162
- 163
- 164
- 165
- 166
- 167
- 168
- 169
- 170
- 171
- 172
- 173
- 174
- 175
- 176
- 177
- 178
- 179
- 180
- 181
- 182
- 183
- 184
- 185
- 186
- 187
- 188
- 189
- 190
- Следующая














